La ciencia aún no ha determinado con total exactitud dónde comienza el alzhéimer en el cerebro. Científicos de la Universidad de Cornell encuentran elementos que apoyan la hipótesis de que comienza en el prosencéfalo basal.
No, el título de este artículo no es un gancho para picar tu curiosidad querido/a lector/a. Si crees que en este punto de la historia de la investigación en el campo del alzhéimer esa pregunta debe estar respondida, te doy la razón. Solo que no es así, al menos no de manera absoluta. Los científicos tienen identificadas áreas del cerebro donde consideran que comienza la enfermedad, solo que algunos dicen que es en una zona y otros que en otra.
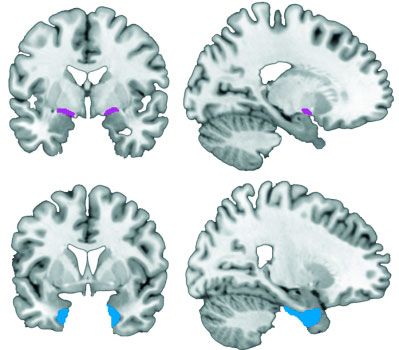
Una investigación recientemente publicada en la revista Nature Communications viene a aportar un elemento de apoyo a los que dicen que el alzhéimer comienza en una región cerebral denominada prosencéfalo basal, en lugar de en las zona de los lóbulos temporales. Más aún, este estudio concluye que la degeneración en el prosencéfalo predice la futura degeneración en los lóbulos temporales.
El prosencéfalo es una estructura cerebral bastante primitiva que está estrechamente ligada a las emociones, la memoria a corto plazo y el aprendizaje. Mientras, los lóbulos temporales, que se ubican encima de nuestros oídos, son fundamentales para la memoria y el lenguaje entre otros muchos procesos cognitivos.
El debate alrededor de dónde comienza el alzhéimer no es vano. Una acertada identificación puede llevar a desarrollar instrumentos diagnósticos tempranos, así como a tratamientos en fases asintomáticas de la enfermedad. Además, este tipo de investigación sigue acumulando evidencia alrededor de la hipótesis de que la enfermedad de Alzheimer se expande como una infección, de unas regiones a otras.
También te puede interesar leer: Síndrome del cuidador quemado. Causas, síntomas y estrategias de afrontamiento.
De una región a otra, como una infección.
Estas conclusiones llegaron después de dos años de estudio de adultos mayores con diferente estatus cognitivo (mental): adultos mayores sanos, otros con deterioro cognitivo leve (DCL) que no evolucionaron a alzhéimer, un tercer grupo que tenía DCL y en un año evolucionó a alzhéimer y; por último, un grupo de enfermos que desde el inicio de la investigación tenía un diagnóstico de alzhéimer.
El DCL es una condición en que la persona manifiesta deterioro de la memoria y otros procesos cognitivos, pero no en grado suficiente como para impedir su normal desarrollo en la vida diaria. Muchas de las personas con DCL nunca llegan a desarrollar demencia, pero otro porcentaje significativo termina recibiendo el temido diagnóstico.
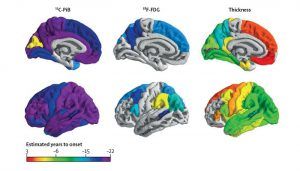
Durante esos dos años de investigación los científicos realizaron, en diferentes momentos, tres resonancias magnéticas de alta resolución a los participantes en el estudio. Comprobaron que, efectivamente, las personas con DCL y alzhéimer tenían una mayor disminución del volumen de la materia gris tanto en los lóbulos temporales como en el prosencéfalo basal. Solo que el deterioro del tejido en este último precedía y pronosticaba la pérdida de tejido en los lóbulos temporales. Para uno de los autores de este estudio, el Dr. Nathan Spreng, la esperanza es:
… que este trabajo lleve un poco de reorganización a este campo en sí mismo, para reevaluar dónde se origina la enfermedad. Eso abriría nuevas vías para la intervención, ciertamente lo hará con la detección”
También te puede interesar leer: ¿Existe relación entre la anestesia y la enfermedad de Alzheimer?
Referencias
Fleischman, B. (2016, November 6). Study challenges model of Alzheimer’s disease progression. Cornell Chronile. Recuperado de http://news.cornell.edu/stories/2016/11/study-challenges-model-alzheimers-disease-progression
Schmitz, T. W., & Spreng, N. (2016). Basal forebrain degeneration precedes and predicts the cortical spread of Alzheimer’s pathology. Nature Communications. doi:10.1038/ncomms13249