El panorama sanitario en relación a las enfermedades neurodegenerativas constituye un reto para los profesionales involucrados en su manejo. La ausencia de medicamentos curativos para la esclerosis lateral amiotrófica (ELA) evidencia la complejidad de esta situación.
¿Por qué no acabamos de encontrar un tratamiento farmacológico curativo para la ELA?
Los medicamentos son formulaciones de moléculas denominadas fármacos, que en base a la evidencia científica son efectivos y seguros para diagnosticar, prevenir o curar enfermedades con el mínimo de riesgos asociados a su uso y el máximo de beneficios.
Hasta el momento no existe una cura para la devastadora enfermedad que nos ocupa. El enfoque farmacoterapéutico orientado a la ELA se restringe al uso de medicamentos para manejar los síntomas asociados al cuadro clínico de modo que el enfoque es puramente paliativo. ¿A qué se debe esto?
La búsqueda de medicamentos efectivos y seguros para tratar una enfermedad parte del conocimiento de los fenómenos a nivel molecular y celular que le dan origen.
Estos resultados tienen una expresión en el organismo que se evidencian en el cuadro clínico propio de cada enfermedad y esto exige una visión amplia e integradora que obliga a un acercamiento multidisciplinario.
Precisamente, la obtención de medicamentos para tratar la ELA se ha limitado por el desconocimiento al detalle de su fisiopatología.
Se han propuesto diferentes hipótesis que no son excluyentes entre sí y apuntan a una multicausalidad que obliga un enfoque de tratamiento con múltiples aristas. Los fármacos buscados deben estar orientados a actuar sobre estas causas y reestablecer las condiciones fisiológicas normales del organismo.
Entre las hipótesis causales de la ELA mejor demostradas tenemos:
- Autoinmunidad.
- Acumulación del neurotransmisor glutamato con efectos tóxicos sobre las neuronas y células de la glía que explican al menos en parte los trastornos celulares de la ELA.
- Estrés oxidativo marcado que agrava los eventos neurotóxicos.
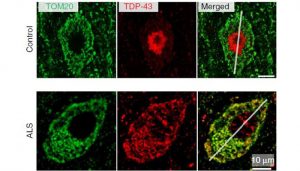
- Degeneración mitocondrial con déficit metabólico.
- Acumulación intraaxonal de proteínas que afectan el transporte y conllevan a la degeneración neural.
De acuerdo a las hipótesis enunciadas se espera cierta efectividad en el tratamiento de la enfermedad de agentes antagonistas del glutamato, de inhibidores de la agregación proteica, de factores de crecimiento, antoxidantes, antiapoptóticos y antiinflamatorios.
Ante el enfoque autoinmune han fracasado hasta el momento los abordajes inmunofarmacoterapéuticos. Una nueva línea de investigación apunta hacia la terapia celular empleando linfocitos T reguladores y células madres con resultados prometedores en fases incipientes de la investigación clínica.
Tratamiento farmacoterapéutico actual de la ELA

Hasta la fecha solo dos medicamentos han logrado el registro de la Agencia Reguladora para Medicamentos y Alimentos de los Estados Unidos de América (FDA) para el tratamiento de la ELA.
El 12 de diciembre de 1995 se aprobó el Riluzol (Comercializado como Rilutek, Glentek y Teglutik) que inhibe la liberación presináptica de glutamato. Por mecanismos moleculares no bien descritos, aumenta la esperanza de vida de los pacientes en 3-6 meses, pero los estudios para correlacionar el tiempo ganado con la calidad de vida son contradictorios.
Este medicamento no es inocuo y tiene asociada una probabilidad de eventos adversos que puede complicar el cuadro clínico de los pacientes.
Las esperanzas actuales se orientan al antioxidante Edaravone (Comercializado como Radicava) que fue aprobado en 2017 por la FDA. Este medicamento ha acumulado evidencia clínica sólida de efectividad como protector de las motoneuronas frente al daño producido por radicales libres.
Sin embargo, este efecto disminuye a medida que progresa la enfermedad y actualmente se discuten sus condiciones de uso cuyo acceso es limitado al paciente por cuestiones de índole económica y comerciales.
Ante este panorama, el único abordaje farmacoterapéutico posible en la práctica clínica cotidiana es el tratamiento sintomático.
Se emplean para esto una amplia gama de medicamentos, algunos de ellos indicados para tratar los eventos adversos que provocan otros, evidenciando cascadas de prescripción complejas que refuerzan la necesidad de una valoración de la relación beneficio-riesgo a conciencia para cada prescripción.
Pueden usarse una amplia variedad de medicamentos para el control sintomático y paliativo. Los inhibidores de la acetilcolinesterasa pueden ser usados por cortos periodos para mejorar la fuerza muscular durante los estadios iniciales de la enfermedad.
Para las alteraciones en el proceso de contracción muscular como las fasciculaciones y la espasticidad se usan sulfato de quinina, carbamazepina, vitamina E, fenitoína, magnesio, verapamilo, baclofen, tizanidina o tetracepan.
Estos pacientes refieren hipersecreción de saliva y se les indica antidepresivos tricíclicos amitriptilina, imipramina que causan resequedad bucal y de paso alivian la depresión ansiosa asociada a la ELA. Los trastornos respiratorios se abordan con broncodilatadores o teofilina.
Sin embargo, cuando consultamos las farmacopeas o los prospectos comprobamos que entre las indicaciones de estos productos no se hace referencia explícita a la enfermedad que nos ocupa.
¿A qué se debe esto? ¿Cómo va la búsqueda de moléculas nuevas que sirvan para tratar la enfermedad?
Perspectivas y retos futuros

La investigación de moléculas prometedoras para el tratamiento de esta enfermedad parte de investigaciones preclínicas en animales de laboratorio.
Los más utilizados se basan en mutaciones de una enzima encargada de desintoxicar al organismo de radicales libres. Los resultados, aunque alentadores, presentan limitaciones serias.
La primera se debe a que la anatomía humana y de los animales es diferente y es complicado extrapolar los resultados de una especie a otra.
Además, la diferencia genética condiciona que la mayoría de los candidatos que han sido prometedores en animales fracasen en el humano y caigan en el “Valle de la Muerte “ de los medicamentos a lo largo de los ensayos clínicos.
Muchas de estas moléculas o formulaciones potencialmente efectivas no se han orientado al blanco farmacológico correcto (receptores, enzimas, tipos celulares específicos, etc) y otras se descartan por deficiencias en los diseños en las fases clínicas de la investigación.
Una mala selección de los pacientes incluidos, un mal escalado del esquema terapéutico que puede implicar subdosificaciones con fracaso por inefectividad o sobredosificaciones con la toxicidad consecuente, han descartado erróneamente alternativas portencialmente beneficiosas para los pacientes con ELA.
Han fracasado por estas causas los ensayos clínicos con vitamina E, selegilina, lamotrigina, Verapamilo, Nimodipino, N-acetilcisteína, la creatina, colecoxib, minociclina, topiramato y otros.
Lograr una estrategia farmacoterapéutica efectiva y segura para la ELA demanda investigaciones en el campo de la clínica, la epidemiología, la genética y la medicina basadas en evidencias sólidas.
Los farmacólogos e investigadores comprometidos en esta meta deben dilucidar la fisipatología molecular de la enfermedad para identificar blancos terapéuticos precisos.
Se hace imprescindible conocer el proceso de desarrollo y la naturaleza de la conectividad neuronal en las áreas cerebrales y espinales afectadas por la enfermedad. Deben desarrollarse también iniciativas de colaboración internacional encaminadas a identificar los factores ambientales que puedan influir en el debut y curso temporal del trastorno.
El diagnóstico precoz, antes de la manifestación de los primeros síntomas, permitirá el diseño y obtención de medicamentos “a la medida” de las necesidades de cada paciente partiendo de la caracterización genética exhaustiva.
Para ello debemos ganar en herramientas para discriminar y evaluar entre todas las moléculas en estudio a las más prometedoras.
Posteriormente a la evaluación preclínica deben optimizarse ensayos clínicos bien diseñados, con la óptima estratificación de los pacientes y con biomarcadores sensibles que permitan evaluar las respuestas farmacocinética y farmacodinámica.
Las enfermedades neurodegenerativas son síndromes complejos con muchos factores asociados a su aparición y progresión.
Más allá de lograr una cura necesaria y milagrosa, la clave de su tratamiento parece recaer en el diseño estrategias abarcadoras que asuma al ser humano enfermo como un todo superior a la suma de sus malestares.
Referencias
Camacho A, Esteban J, Paradas C. Report by the Spanish Foundation for the Brain on the social impact of amyotrophic lateral sclerosis and other neuromuscular disorders. Neurologia. 2015; S0213-4853(15)00034-1
National Institute of Neurological Disorders and Stroke. Amyotrophic Lateral Sclerosis (ALS) Fact Sheet. [En línea]. [Consultado en Noviembre de 2018] https://www.ninds.nih.gov/
Rix Brooks et al. Edaravone in the Treatment of Amyotrophic Lateral Sclerosis: Efficacy and Access to Therapy— A Roundtable Discussion Am J Manag Care. 2018;24 : S175-S186