Entrevista a Iñaki Osorio Querejeta, investigador en el Instituto de Investigación Sanitaria Biodonostia en el área de la esclerosis múltiple. Iñaki busca cerrar el paso a la desmielinización, o más bien reconstruir lo que la EM ha destruido. Y lo hace yendo en sentido contrario a la enfermedad: remielinizando.
Empecemos por las bases, aclarando los tres conceptos que mencionaremos una y otra vez en esta entrevista: ¿qué es la mielina? ¿qué es la desmielinización? Y por último, ¿qué es la remielinización?
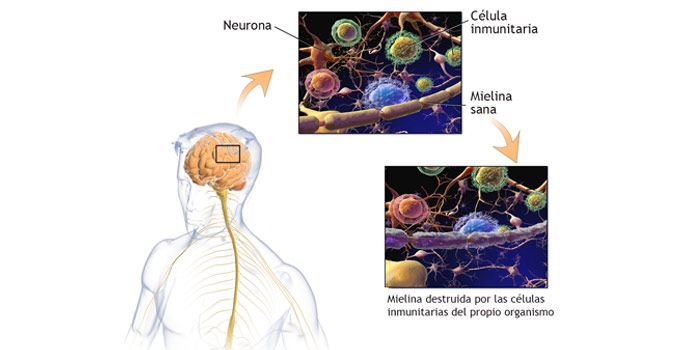
La mielina es una capa lipoproteica formada por los oligodendrocitos en el sistema nervioso central y que envuelve a los axones. Principalmente tiene dos funciones: por un lado nutre y protege a los axones y por el otro permite que la transmisión del impulso nervioso se produzca de manera adecuada.
La desmielinización es un proceso por el cual se daña la vaina de mielina que recubre los axones. Esto provoca que la transmisión del impulso nervioso no se lleve a cabo de manera adecuada, además de quedar el axón desprotegido pudiendo dar lugar a la pérdida del mismo.
En la esclerosis múltiple, en los primeros estadios de la enfermedad, el 80% de los pacientes tienen la capacidad de regenerar esa mielina perdida antes de que el axón muera, en un proceso denominado remielinización.
En las lesiones desmielinizantes se liberan una serie de sustancias que atraen a las células precursoras de oligodendrocitos, que migran hasta las lesiones, proliferan y se diferencian a oligodendrocitos, los cuales generaran nueva mielina alrededor del axón.
Biológicamente, ¿podrías describirnos cómo es el proceso que lleva a la desmielinización en la esclerosis múltiple (EM)?
Si bien no está claro que factores son los desencadenantes de la enfermedad, hoy en día sabemos que el daño en la mielina se produce por una respuesta inmune aberrante. La función del sistema inmune es la de protegernos frente a agentes externos como por ejemplo los virus y las bacterias.
En la esclerosis múltiple el sistema inmune detecta a la mielina como un agente externo y dañino frente al cual debe protegernos. Y es entonces cuando se produce una respuesta inmune frente a la vaina de mielina que tiene como consecuencia la desmielinización característica de la enfermedad.
A nivel sintomático, ¿cómo se manifiesta ese daño a la mielina?
La manifestación clínica dependerá de las regiones lesionadas. Podríamos definir que los síntomas más frecuentes en los pacientes son alteraciones visuales, problemas de movilidad, alteraciones de sensibilidad y el habla, alteraciones sexuales y trastornos cognitivos y emocionales entre otros.

Los niveles crecientes de discapacidad que experimentan algunas personas con EM, ¿son consecuencia directa de la desmielinización o hay otros mecanismos involucrados?
Por lo general, el aumento progresivo de la discapacidad se asocia con procesos neurodegenerativos. Estos son los que tienen lugar cuando los axones quedan al descubierto tras una lesión desmielinizante y mueren.
Si bien la neurodegeneración se había asociado con estadios avanzados de la enfermedad en las formas remitentes recurrentes, nuevos estudios parecen indicar que esta neurodegeneración también tiene lugar, aunque en menor medida, en los estadios tempranos.
Una vez la capa de mielina se daña, ¿qué sucede? ¿el propio organismo tiene capacidad para repararla o es un daño permanente?
Como hemos mencionad antes, tras producirse una lesión desmielinizante se liberan una serie de señales que atraen a las células precursoras de oligodendrocitos hasta las lesiones. Estas proliferan y se diferencian a oligodendrocitos, que son los responsables últimos de generar nueva mielina.
Con la evolución de la enfermedad, esta capacidad del organismo para regenerar la mielina decae. No está claro porqué se pierde la capacidad remielinizante, pero parece estar relacionada con una falta de las células precursoras de oligodendrocitos, una insuficiente migración, una diferenciación inadecuada.
Actualmente, ¿hay alguna opción terapéutica que favorezca la remielinización en casos de lesiones crónicas?
En la actualidad no existe ningún fármaco comercialmente disponible cuyo objetivo sea la remielinización. Se trata de un campo difícil, pero en el cual tanto las empresas farmacéuticas como los investigadores están apostando fuerte.
Cabe destacar que la remielinización es importante que se dé en los primeros estadios tras producirse la lesión desmielinizante, dado que si el axón permanece mucho tiempo desnudo puede degenerar y morir. Si el axón muere, ya no es posible que se dé la remielinización.
Por ello creemos que en un futuro en el cual esté disponible una terapia remielinizante eficaz, sería muy importante administrarla desde las primeras fases de la enfermedad junto con una terapia que evite el daño, como las que actualmente existen en el mercado.
De esta manera pensamos que podríamos tener la enfermedad controlada y evitar en cierta medida la neurodegeneración.
En el campo investigativo y teniendo en cuenta el objetivo terapéutico de alcanzar la remielinización, ¿qué líneas de investigación son las más prometedoras en el panorama actual?
Las claves para el desarrollo de una terapia remielinizante pasan por fomentar y estimular los procesos que se ven deteriorados en los estadios en los cuales la remielinización no tiene lugar. Es decir, suplir la falta de células precursoras de oligodendrocitos, promover la diferenciación de estas células, estimular su migración y favorecer su proliferación.
Para ello se están abordando diferentes estrategias. Por un lado, la utilización de células madre podría suplir la falta de células precursoras de oligodendrocitos.
Por otro lado, se está trabajando con fármacos y pequeñas moléculas con el fin de estimular la diferenciación de estas células. Es, por ejemplo, el caso del Anti-lingo, un fármaco prometedor que sin embargo no ha demostrado su eficacia en un ensayo clínico de tipo III.
En la actualidad también se están realizando estudios con vesículas extracelulares. Estas vesículas son un sistema de comunicación intracelular y que parece que bajo ciertas condiciones podría promover la mielinización.
Como he citado previamente, la comunidad científica está haciendo un gran esfuerzo y esperamos que esto pueda traducirse en el desarrollo de terapias remielinizantes.
Estás realizando tu doctorado en la Unidad de Esclerosis Múltiple del Instituto de Investigación Sanitaria Biodonostia, ¿qué estáis investigando en relación a la EM?
Así es, estoy realizando la tesis doctoral en el Instituto de Investigación Sanitaria Biodonostia. Mi tesis consiste en la utilización de microRNAs como potenciadores de la remielinización. Los microRNAs son unos RNAs pequeños que están involucrados en la regulación celular.
Nuestra hipótesis consiste en que la utilización de ciertos microRNAs podría modificar una serie de rutas celulares que finalmente estimularían la generación de nueva mielina.
Para ello trabajamos con diferentes modelos experimentales de la enfermedad. Uno de ellos consiste en la obtención de células precursoras de oligodendrocitos en las que, tras ser cultivadas, se procede a la administración de los microRNAs y estudiamos el efecto que producen estos en las células.
Por otro lado, también tenemos proyectos en los cuales estudiamos la senescencia del sistema inmunitario en relación con la esclerosis múltiple, profundizamos en el descubrimiento de nuevos biomarcadores en la EM y estudiamos la implicación de la microbiota en la EM como miembros del consorcio internacional para el estudio de la microbiota en pacientes de esclerosis múltiple.
También te puede interesar leer: Síndrome de desmielinización osmótica, una complicación que el médico puede evitar