LMTX®, un fármaco en fase de ensayo clínico para la demencia frontotemporal, recibió recientemente la designación de medicamento huérfano de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA).

Para quienes estén familiarizados con el campo de la demencia, el fármaco LMTX® no les resultará desconocido; lleva muchos años en fase experimental intentando vencer el alzhéimer.
Por el momento los resultados no han sido los esperados, pero continúa siendo evaluado en ensayo clínico.
Por su mecanismo de acción, que apunta a evitar la acumulación de determinadas proteínas en el cerebro de los enfermos (uno de los mecanismos más frecuentes de las enfermedades neurodegerativas), LMTX® también ha sido visto como un candidato atractivo a tratar la demencia frontotemporal variante conductual (DFTvc).
La DFTvc es un síndrome que se manifiesta generalmente antes de los 60 años y provoca marcadas alteraciones de conducta; por ejemplo, el afectado puede mostrarse impulsivo, desinhibido, falto de empatía y en muchos casos con una profunda apatía.
Recientemente la FDA estadounidense designó a LMTX® como medicamento huérfano, un categoría que «alienta a las empresas a crear productos al ofrecerles incentivos financieros y de otra índole».
Se concede a medicamentos destinados al tratamiento, diagnóstico o prevención de enfermedades raras o trastornos que afectan a menos de 200,000 personas en los EE. UU o que afectan a más de 200,000 personas pero que no se espera que recuperen los costos de desarrollar y comercializar un tratamiento farmacológico.
También te puede interesar leer: LMTX , fármaco en desarrollo para el alzhéimer, vuelve a dar señales de vida
¿Qué es LMTX®?
Es un inhibidor de la agregación de la proteína tau, lo que esencialmente significa que busca impedir que en el cerebro de los enfermos se acumulen proteínas (tau) que resultan tóxicas a las neuronas.
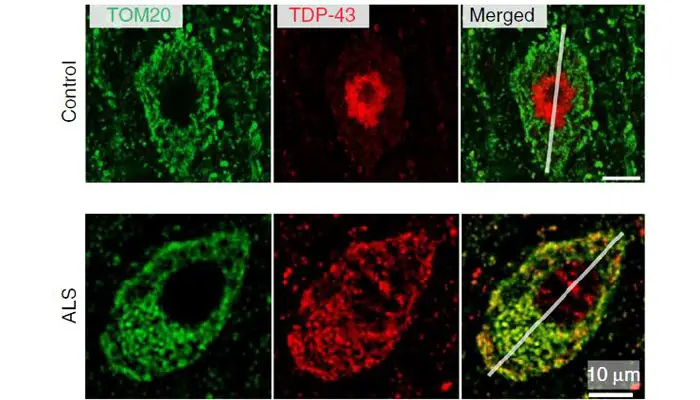
Aunque este es su mecanismo de acción primario, también se ha observado, según comentan desde TauRx, que puede inhibir la agregación de otra proteína, la TDP-43.
Tanto la agregación de tau como TDP-43 tienen un papel fundamental en los diferentes subtipos de demencia frontemporal, incluyendo la variante conductual.
También te puede interesar leer: Fármacos y alzhéimer: LMTX o Rember ¿Una gran promesa o una promesa real?
¿Qué se conoce hasta ahora de LMTX® en la demencia frontotemporal?
Ya se ha realizado un ensayo clínico con el fármaco en 220 pacientes con DFTvc, los resultados se conocieron en septiembre de 2016.
En el ensayo, a un grupo de pacientes se le administró una dosis de 100 mg dos veces al día de LMTX® mientras a otro grupo (el que tomaron como control) se le administró 4 mg dos veces al día.
Al finalizar el estudio los investigadores no detectaron diferencias significativas entre los grupos, con lo cual la eficacia del fármaco no quedó demostrada.
Sin embargo, las esperanzas sobre LMTX® se mantienen debido a que los investigadores concluyeron que los pacientes que participaron en el estudio tuvieron un menor deterioro cognitivo que el reportado en otros estudios con pacientes con DFTvc.
Pero esas comparaciones son insuficientes para hablar a favor de la eficacia de un fármaco y aunque LMTX® respira, todavía tiene un largo camino por delante antes de decir que puede ayudar a las personas afectadas por demencia frontotemporal.
También te puede interesar leer: AL001, el fármaco experimental para la demencia frontotemporal que recibió la designación de medicamento huérfano de la FDA
Fuentes
NIHR: Leuco-methylthioninium (LMTX) for behavioural variant frontotemporal dementia – first line. En http://www.io.nihr.ac.uk/wp-content/uploads/migrated/2496.ab7b2d40.TauRx_LMTX_Sep13.pdf
TauRx Therapeutics Ltd (2016). En http://taurx.com/trx-237-007-phase-3-clinical-trial-update.pdf
TauRx Therapeutics Ltd (2018): FDA Grants Orphan-drug Designation for TauRx’s LMTX in Frontotemporal Dementia. En https://markets.businessinsider.com/news/stocks/fda-grants-orphan-drug-designation-for-taurx-s-lmtx-in-frontotemporal-dementia-1027792672