El pasado diciembre la FDA estadounidense aprobó la comercialización de INBRIJA™, una terapia para los periodos Off en el párkinson. La compañía que desarrolló la terapia ya presentó una solicitud de autorización de comercialización ante la Agencia Europea de Medicamentos (EMA) el pasado 23 de marzo.

En EE.UU ya puede comercializarse INBRIJA™, una terapia para los episodios OFF que experimentan alrededor de 420 000 enfermos de párkinson solo en Europa.
El pasado diciembre la FDA estadounidense dio luz verde a la salida de la terapia al mercado y se espera que esté llegando a las farmacias del país norteamericano durante el primer trimestre de 2019.
INBRIJA™ no es un fármaco nuevo, de hecho, es levodopa, el fármaco que lleva décadas siendo la principal terapia para los enfermos de párkinson.
La peculiaridad de INBRIJA es su forma de administración, que se realiza mediante inhalación oral, semejante a como se administran varias terapias para el asma.
De esta forma se consigue evitar el paso del fármaco por el sistema gastrointestinal acelerando así su acción.
También te puede interesar leer: Son para otras enfermedades, pero estos fármacos podrían llegar a tratar el párkinson: el reposicionamiento gana fuerza en la EP
¿Para qué está indicado INBRIJA?
La terapia está indicada para el tratamiento de los periodos OFF en los pacientes de párkinson.
Estos episodios se van haciendo más comunes a medida que avanza la enfermedad y se expresan mediante el surgimiento de síntomas motores de párkinson a pesar de que el paciente tenga optimizado su tratamiento.
INBRIJA es una terapia para ayudar a controlar los síntomas de los episodios OFF en las fluctuaciones motoras, no una terapia curativa ni que cambie de algún modo el curso de la enfermedad.
¿Cómo se administra?
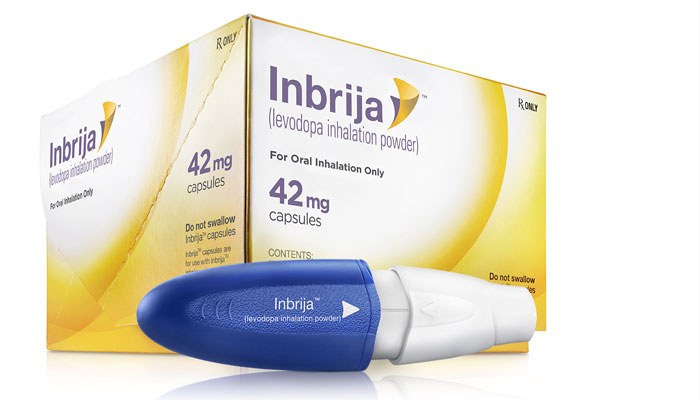
La terapia es autoadministrada y su aplicación depende de las necesidades del paciente (es decir, él mismo decidirá cuándo usarla, siguiendo la prescripción y las orientaciones de su médico)
Se administra mediante un inhalador específico (ver imagen anterior) al que se le introducen dos píldoras por cada dosis y no se recomienda usar más de 5 veces al día.
Desde Acorda Therapeutics, la farmacéutica que ha desarrollado la terapia, insisten en que es muy importante que los pacientes nunca tomen las píldoras, sino que estas se administren mediante el inhalador.
También te puede interesar leer: Tratamiento de los episodios Off en el párkinson avanzado: comenzarán a probar en Europa tiras sublinguales en el tercer trimestre de 2016
¿Qué reacciones adversas se han descrito?
La reacción adversa más común es tos, que según se ha observado en ensayo clínico, puede llegar a afectar hasta el 15% de los pacientes tratados con INBRIJA.
Le sigue en frecuencia las infecciones del tracto respiratorio superior, las náuseas y el esputo descolorido.
¿Cuándo puede estar disponible INBRIJA en España?

La disponibilidad de la terapia en España depende de si la Agencia Europea de Medicamentos da una recomendación positiva sobre su comercialización.
El pasado 23 de marzo la compañía presentó ante la EMA su solicitud para comercializar INBRIJA y está a la espera de la respuesta del organismo regulador, que se debe producir en el primer trimestre de 2019.
También te puede interesar leer: La levodopa inhalada para el párkinson pasa a ser evaluada por la FDA
Fuentes
Acorda Therapeutics, Inc. (2018): Acorda Announces EMA Validation of the MAA Submission for INBRIJA™ (levodopa inhalation powder). En http://ir.acorda.com/investors/investor-news/investor-news-details/2018/Acorda-Announces-EMA-Validation-of-the-MAA-Submission-for-INBRIJA-levodopa-inhalation-powder/default.aspx
Acorda Therapeutics: INBRIJA™ (levodopa inhalation powder).En http://www.acorda.com/products/products/inbrija
Web oficial del fármaco localizada en https://www.inbrija.com/